La batería de un coche es su fuente de energía. La batería, a menudo rectangular y con forma de caja, es el almacén de electricidad que un vehículo necesita para arrancar el motor y mantener la carga. Además del motor de arranque, las bujías, las luces y demás aplicaciones de índole electrónica requieren energía eléctrica. Pero, ¿de qué está hecha una batería? ¿Y cómo funciona realmente?
¿Qué es una batería de coche?
Por fuera, la batería de un coche parece un aburrido bloque plasticoso con algunos conectores en la parte superior. Pero esa cubierta exterior de polipropileno es bastante dura y, por lo general, resistente a los ácidos. Asimismo, protege el complejo funcionamiento interno y los materiales de los que se compone para hacer magia. Porque el interior de la batería alberga una solución química (generalmente ácido sulfúrico) y varias capas de placas de plomo y dióxido de plomo que reaccionan con el ácido para crear energía.
Las baterías de coche se venden con diferentes niveles de voltajes, siendo las más típicas las de 12 voltios. Bueno, para ser exactos, las baterías de 12,6 V contienen seis celdas, cada una de las cuales produce 2,1 V en un estado de carga completa. Por eso, cada disminución de 0,2 V en la carga de una batería equivale a, aproximadamente, 25 % de pérdida de su energía. Por lo tanto, es fundamental mantener el estado de la carga adecuada de la batería en todo momento. Por eso hay que tener en cuenta algunos aspectos para no agotarla antes de tiempo.
Además, la batería del coche también se encarga de mantener constante la corriente eléctrica. Porque la batería no solo proporciona la energía necesaria para arrancar un vehículo, sino que también estabiliza el voltaje (ese es el término para el suministro de energía) para mantener el motor en funcionamiento. Prácticamente todas las funciones del coche dependen de la batería que tan poco solemos mirar. Llámalo, “la pequeña caja de energía”, aunque suelen superar los 10 kilos de masa sin problema alguno.
¿Cómo se estructura una batería de coche?
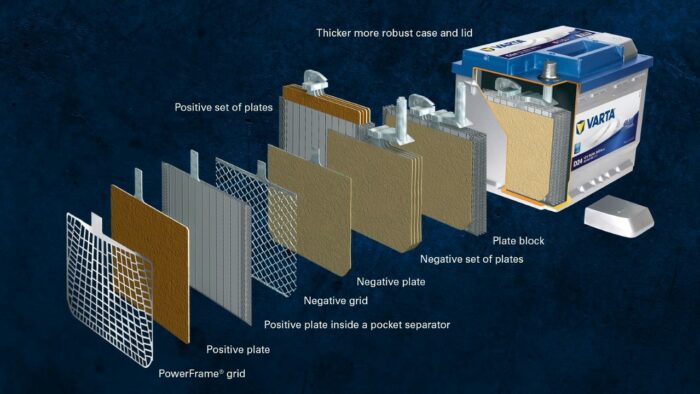
En combinación a los materiales recién descritos, y la razón por la cual son tan pesadas, una batería de coche se estructura en torno a dos elementos:
- Electrodo positivo: en una batería de plomo-ácido, la placa con carga positiva (material activo) consta de óxido de plomo (PbO2) que se sumerge en un electrolito. Esta se usa para contener el material activo y como colector de corriente.
- Electrodo negativo: la placa cargada negativamente consiste en plomo puro (Pb), que también se encuentra sumergido en un electrolito. Al igual que la placa positiva, esta también consiste en una aleación de plomo y tiene el mismo propósito.
Los electrodos con diferentes cargas están separados por una bolsa separadora. El electrolito es una mezcla de ácido sulfúrico (H2SO4) y agua destilada. Ese electrolito puede estar en forma líquida (como en las baterías húmedas convencionales), en forma de gel o ligado en una malla de vidrio. Varios electrodos positivos forman un grupo de placas positivas, mientras que varios electrodos negativos forman un conjunto de placas negativas. Todos juntos forman un bloque de placas que, en conjunto, forman la celda de la batería.
Una regla común en cualquier batería de este tipo es: cuantas más placas contenga una celda y, por lo tanto, formen una superficie más grande, mayor será la potencia de arranque en frío que puede entregar la batería. Sin embargo, si el espacio en la celda se usa para menos placas, pero más gruesas, la estabilidad del ciclo aumenta, lo que significa que la batería está diseñada para un mayor rendimiento de carga (proceso continuo de carga y descarga). Esas celdas están en una carcasa con un sistema de laberinto que evita fugas indeseadas.
¿Cómo funciona la batería de un coche?
Como decíamos, una batería de un coche almacena energía en forma química y la convierte en energía eléctrica. En este proceso electroquímico, existen cuatro materiales reaccionan entre sí: hidrógeno (H), oxígeno (O2) plomo (Pb) y azufre (S). La conexión de un consumidor externo inicia la reacción química en la batería, como veremos a continuación:
El electrolito, esa mezcla de ácido sulfúrico (H2SO4) y agua destilada, se descompone en iones de hidrógeno con carga positiva (H+) e iones de sulfato con carga negativa (SO4 2-). Al mismo tiempo, los electrones (2e-) viajan del electrodo negativo al positivo a través del consumidor externo. Para compensar ese flujo de electrones, los iones de sulfato viajan desde el electrolito hacia el electrodo negativo, donde reaccionan con el plomo (Pb) para generar sulfato de plomo (PbSO4).
El sulfato de plomo también se produce en el electrodo positivo, donde el enlace de oxígeno (O2) en el óxido de plomo (PbO2) se rompe por la transferencia de electrones y el oxígeno pasa al electrolito. El plomo restante (Pb) se une con el sulfato (SO4) del electrolito. Allí, el oxígeno se une al hidrógeno para formar agua (H2O). A medida que el ácido sulfúrico se consume por la formación de sulfato de plomo, la concentración de la solución electrolítica se reduce. Cuando la concentración de ácido cae por debajo de un cierto nivel, la batería debe recargarse.
Durante el proceso de carga, los procesos químicos tienen lugar en secuencia inversa. Al final, se pueden encontrar los elementos originales. Decíamos que el electrodo positivo consiste en sulfato de plomo (PbSO4), el electrodo negativo consiste en plomo completamente puro (Pb) y el electrolito consiste en ácido sulfúrico diluido (H2SO4). Como este proceso de conversión está asociado con pérdidas, una batería solo puede soportar un número limitado de ciclos de carga. Su vida útil es, por lo tanto, limitada, razón por la que hay cambiarla cada varios años.